
 |
|
|
Главная --> Промиздат --> Абразионные материалы в присутствии металлич. электрода, одноименного с осаждаемым ионом, напр. серебряного электрода в растворе AgNOg; 3) титрование в присутствии необратимого электрода, погруженного в раствор. Эти способы уже ра.зработаны для осаждений, окислений, восстановлений и нейтрализации (к 1924 г. не Meffee 60 различных примеров потенцио-метрического титрования). Во всех этих случаях каждый прибавленный см или каждая капля отмечаются на оси абсцисс, а измеренные при этом потенциалы - на оси ординат. В момент переходной точки происходит резкое изхменение потенциала. Анализ органических соединений отличается от неорганич. анализа тем, что определение содержания элементов производится сравнительно легко; но большие затруднения встречаются, когда нужно разобраться в смеси органич, соединений. Определение углерода делается путем сжигания вещества в токе кислорода или воздуха с улавливанием продуктов горения; при этом присутствие водорода обнаруживается благодаря образованию воды; азот определяют прокаливанием вещества с металлич. натрием: при этом за счет азота образуются цианистые соединения натрия. Гораздо труднее выяснить детальный состав органич. смеси. Для отделения друг от друга ингредиентов такой смеси прежде всего применяется действие растворителей, т. к. вода (как вещество сильно ассоциированное) растворяет вещества в свою очередь сильно ассоциированные (напр. спирты, к-ты) и не переводит в раствор слабо ассоциированные вещества (напр. эфиры, углеводороды и т. п.); зато последние хорошо растворимы в гексане и в бензоле. После достаточного очищения органич. вещества возможно приступить к количественпому анализу его, что производят сжиганием до COg, HgO, Ng, SO2 и т. д. Наиболее удобно это производить в калориметрических бомбах, т. е. в кислороде под большим дав.тением. В последнее время все чаще и чаще применяются также и короткие сожигательные трубки, и при этом газы пропускают для сожжения через трубки с накаленным платинированным асбестод! (способ Деннштедта), но обычно применяют длинные трубки, наполненные прокаленной окисью меди, и сожжение ведется в струе кислорода. Выходящие из прибора газы пропускают: 1) через хлор-кальциевую трубку или змеевичок с HgSO.- для поглощения воды, 2) через прибор с крепкой щелочью (калиаппарат)-для поглощения СО2- Азот, если его молено выделить в виде аммиака при нагревании с натронной известью, определяют осаледением в виде хлороплатината аммония; в противном случае азот может быть определен после сожжения в виде непоглощенного остатка газа измерением объема последнего; или же нагреванием с серной к-той переводят азотистое соединение предварительно в сернокислый аммоний, а затем улсе, обработав избытком едкого натра, отгоняют аммиак. Хлор определяют нагреванием с азотной кислотой и AgNO в виде AgCl. Анализ физиологических веществ еще труднее, чем органический. и основан на ряде практических наблюдений. Очень широко распространен микрохимический анализ, к-рый часто производят над ничтолсными долями вещества, руководствуясь формой кристаллов или некоторыми характерными реакциями. Микрохимический анализ приходится особенно часто применять п])и судебных экспертизах, когда необходимо разреншгь задание на основании ничтожных следов или остатков вещества, попадающих в распоряжение следственных властей. В техническом анализе обычно преследуется не столько точность, для достилсения к-рой требуется очень много времени, сколько скорость выполнения анализа. При этом оказывается возлюжным использовать результаты хотя и с допущением ошибок, лишь бы эти ошибки при одинаковых условиях имели ту лее самую величину и тот лее самый смысл. Вот почему при технич. ана.лизе методы обычного ко.личествен-ного анализа, построенного на взаимодействиях, идущих до конца и в основе своей соответствующих качественному анализу, заменяются иногда методами, к-рые пе дают точного выполнения теоретической реакции, но зато быстро и всегда одинаково выполнимы. Сейчас широко разрабатываются стандартные способы технич. диализа. При этом устанавливается самый прием взятия пробы, к-рую часто приходится брать от больших партий и уменьшать до необходимых для лабораторной работы размеров. В последнее время стараются в технич. анализе заменить весовые приемы объемными и колориметрическими; последние основаны на сравнении интенсивности окраски определенного слоя исследуемого раствора с интенсивностью окраски такого лее слоя раствора с известным содерлеа1шем растворенного вещества (стандартный раствор). Понятно, что иногда такое исследование можно вести непосредственно для окрашенного вещества, иногда (напр. для солей меди или железа) нужно перевести исследуемые соединения в окрашенные соединения. Обычно сравнивают изучаемый раствор с определенным слоем основного раствора и изхменяют высоту слоя раствора, пока не получится при рассматривании сверху обоих растворов одинаковый оттенок; или лее ищут ту толщину слоя, при к-рой цвет раствора уничтожается наложением определенной, окрашенной в дополнительный цвет п.ластин-ки. Специальным примером колориметрического анализа является также метод определения серы по окрашиванию фильтра сернистым кадмием, выделенным из определенного объема раствора. Иногда возможно определять содерлеание какого-нибудь вещества в растворе (но, конечно, если отсутствуют другие посторонние примеси) по П.ЛОТНОСТИ, напр. ареометром (см. Денсиметрия); так же определяется число градусов спиртового раствора сниртометро. (см. Алкоголеметрия). Для растворов двух чистых веществпользуются рефрактометрией, т. е., составив заранее таблицу изменений показателя преломления в зависимости от состава двух составных частей раствора, по показателю преломления определяют состав данной смеси. Этим пользуются и в технич. анализе для определения масел. Для растворов Сахаров и некоторых белковых веществ можно использовать п о-ляриметрию, т. е. измерение величины вращения поляризованного света в данном растворе. При исследовании органич. веществ широко пользуются наблюдениями над температурами кипения, над изменениями их во вре.\1я перегонки и температурами плавления, которые для каждого вещества являются вполне опреде.пенными константами. Это, в сущности, наилучший способ анализа смеси летучих веществ, если в нашем распоряжении имеется большое количество исследуемой смеси и если молено вести фракциоиировку, пользуясь хорошим дефлегматоро.м. Очень широко распространены металлографический и микроминералогический анализы, т. е. наблюдение тонких шлифованных пластинок исследуемого вещества под микроскопом. В микроминералогиче-ском анализе широко применяется наблюдение в поляризованном свете при помощи т. н. по.пяризационного микроскопа, что облегчает определение отдельных минералов в исследуемой горной породе. На основании кристаллографических и оптических свойств возмолсен кристаллохимический анализ. Анализ металлографический в 1Ш очень сложных случаях, ггапр. для углеродистой стали, содержащей мало примесей, позволяет определять состав материала с большой точностью по соотношению площадей па шлифе, занятых ферритом и перлитом в сполна отпущенной стали. При изучении сплавов металлографический анализ соединяют с термическим анализом, т. е. определением хода охлаждения сплава при помощи термоэлемента или термометра. Эти данные на основа! гии правила фаз позволяют судить об изменениях, происходящих в сплаве, преимуществегшо об образовании химических и кристаллических соединений определенного (дальтонидов) и неопределенного (бертоллидов) состава. К термическому и металлографическому анализам обычно присоединяют: 1)магнитометриче-с к и й, т. е. измерение магнитных свойств, преимущественно железных, кобальтовых и никелевых сплавов; 2) термоэлектрически й, т. е. определение электровозбудительной силы данного сплава относительно чистого вещества; 3) кондуктоме-трический - определение электропроводности сплавов; 4) определение температурного коэффициента электропроводности; 5) определение твердо-с т и; 6) определение текучести и т.д. Все эти методы позволяют определять наличие И.ПИ отсутствие т. н. особых точек , характеризующих то или иное строение сплава: кристаллические растворы, эвтектики, кристаллические соединения. Совершенно так же для определения особых точек в жидких растворах применяют аналитические методы, основанные на зависимости от состава исследуемой смеси: 1) плотности, 2) первой производной плотности, 3) упругости пара, 4) темп-р кристаллизации, 5) темп-р кипения, 6) вязкости, 7) коэфф-тов расширения и т. д. Для определения состава кристаллогидратов и кри-сталлоаммиакатов наблюдают упругость пара в зависимости от состава при постоянной t°, имея в виду, что для достаточно прочных кристаллов упругость пара постоянна, пока состав cobokvuhocth постоянен. Лит.: Тредвелл Ф. П., Качественный анализ, ГИЗ, 1923; М е н ш у т н и н Н. А., Аналптич. химия, ГИЗ, 1922; Тредвелл Ф. П., Таблицы качеств, хим. анализа. Л., 1924; Дёрипг Т., Обзор работ по .аналит. химии, вып. 1 - 1914-19 гг., 1922; Тананаев Н. А., Капельный метод качественного химического анализа, Л., 1926; Ш т а уд и н г е р Г., Органический качественный анализ, Л., 1926; Федотьев П. П., Технич. анализ минеральных веществ, вып. 1-5, 1922-1926; Э м их Ф., Микрохим. анализ, Л., 1926; Ztschr. f. analyt. Chemie*, Munchen; Kolthoff I. M., Der Gebrauch v. Farbenindikatoren, 1923; Kolthoff I. M., Die .Massenanalyse, В., 1927. В. Курбатов. АНАЛИТИЧЕСКАЯ ГЕОМЕТРИЯ, отрасль математики, занимающаяся гео.метрически-ми исследованиями при помощи методов алгебры и анализа. А. г. основана на определении положения точек в пространстве при помощи чисел, называемых координатами. На плоскости выбирают неподвижную точку О и две пересекающиеся прямые ОХ и OF (координатные оси) (фиг. 1). Положение любой точки Р на п л о-скости определится, если разложить отрезок ОР на два составляющих отрезка 0Q и QP, параллельных координатным осям, или OR и RP. Число X, выралеаюшее длину отрезка 0Q, называется абсциссой ражающее длину отрезка ординатой той же и у резки 0Q и QP направлены в те лее стороны, что и соответствующие оси ОХ и 0Y, и отрицательнььми, если они обращены соответственно в противопололсную сторону. При эгих соглашениях каждой точке на плоскости отвечают вполне определенные значения абсциссы ж и ординаты у и обратно, каждой паре значений х и у отвечает одна точка на плоскости. Абсциссы и ординаты носят общее название координат точки Р. Обычно угол между координатными осями берется прямой, тогда составляющие 0Q и QP вектора ОР являются его прямоугольными проекциями (ортогональные координаты). Эгот способ координации (определения по.по7кения точки) был указан Декартом (1637 г.), и поэтому самые координаты нося г название декартовых. Можно определять положение точки Р иа плоскости также и при помощи полярных координат, указывая длину отрезка ОР=г и угол & между осью ОХ и вектором ОР. 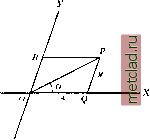 Фиг. 1. точки Р, а число у, вы-QP, называется точки. Числа х считаются положительными, если от- АНАЛОГИЧЕСКИЙ НОЛЮС
Положение точки Р в пространстве определяется при помощи трех чисел. Через точку О проводят три непараллельных одной плоскости прямых ОХ, О Г, 0Z и разлагают ОР на составляющие, параллельные этим прямым (фиг. 2), Здесь каждой координате также присваивается знак в зависимости от того, совпадает ли составляющий отрезок с направлением соответствующей координатной оси или же имеет противоположное направление. Положительные или отрицательные числа, равные этим составляющим, обозначаются обыкновенно буквами X, у, Z называются коор-2 динатами точки Р в пространстве. Чаще всего берут три взаимно перпен-дику.тярные оси ОХ, 0Y и 0Z. Тогда составляющие радиуса-вектора ОР становятся равными прямоугольным проекциям его на координатные оси, а соответствующие числа X, у, Z называются прямоугольными координатами точки Р или радиуса-вектора ОР. Пололсение точки Р в пространстве м. б. определено и другими координатами. Можно, напр., построить сферу с центром в О, проходящую через точку Р, и выбрать на этой сфере экватор и начальный меридиан. Тогда сферическими координатами точки Р называют три числа: радиус сферы, широту и долготу точки Р. Число координат, необходимых для полного определения положения точки Р, равно числу измерений рассматриваемого пространства. Для исследования геометрич. свойств различных фигур в пространстве и их взаимного расположения надо выразить эти свойства при помощи ур-ий, связывающих между собой координаты точек, принадлелеащих этим фигурам. Например координаты всех точек сферы с центром в О удовлетворяют ур-ию а 4- г/* -Ь з* = (где R - радиус сферы), ибо квадрат радиуса-вектора равен сумме квадратов его проекций. В общем виде ур-ие f{x, t/,z) = О выражает нек-рую п о-верхность. На плоскости можно предположить Z = 0; тогда ур-ие f{x, у) = О выражает нек-рую линию, т. к. это ур-ие м. б. решено относительно одной из координат: у = fix), при. чем каждому значению X соответствует одно или несколько значений у, а следовательно,-определенные точки на плоскости. Обратно, каждая кривая может быть выражена ур-ием между координатами ее точек. Целый ряд геометрич. задач м. б. разрешен при помощи алгебраич. вычислений. Напр., если даны две кривые в ур-иях fix, у) = 0 и Fix, у) = 0, то для нахождения точек пересечения этих кривых достаточно решить совместно эти два уравнения. Полученные значения координат X и у будут координатами точек пересечения. Во многих задачах целесообразно не определять радиусы-векторы различных точек при помощи координат, а вести вычисления непосредственно над радиусами-векторами этих точек при помощи методов векторной алгебры. Этот метод имеет большие преимущества для исследования линейных фигур, прямых линий, плоскостей и их взаимного расположения. Методы А. г. имеют громадное значение для разрешения задач механики и физики. Лит.: М Л О д 3 е е В С к и й Б. К., Основы аналитич. геом. на плоскости, ГИЗ, 1923; с г о ж е. Основы аналитич. геом. в пространстве, М., 1924; Соколовский И. И., Аналитич. геометрия в векторном изложении, Москва, 1926; Поляков А. П., Аналитич. геом., 1926; Цубербиллер О. П., Сборник задач и упражнений по аналитич. геом., ГИЗ, М., 1 927. Я. Шпильрейн. АНАЛОГИЧЕСКИЙ ПОЛЮС, конец кристалла, электризующийся положительно при повышении температуры (температура и потенциал увеличиваются или уменьшаются одновременно). Противоположный конец кристалла, электризующийся отрицательно, называется анталогическим полюсом. АНАМОРФИЗМ, явления изменения горных пород, связанные с эндотермическими реакциями и реакциями диссоциации, происходящие под влиянием высоких давлений и t°, существующих в глубинных зонах земной коры. Явления А. тесно связаны с явлениями динамо метаморфизма (см.). В результате А. происходит образование силикатов, безводных соединений и ряд восстановительных процессов. Английский геолог Ван-Хайз (Van Hise) противополагает зоне А. зону катаморфизма, объединяющую пояса разрыхления и цементации. АНАНАСНАЯ ПЕНЬКА, волокно, из листьев различных видов ананаса и родственных ему растений; разводится на Вест-Индских о-вах, в Ц. Америке, на Филин-пинах, на о-ве Формоза. Волокно А. п. отличается тониной, блеском, шелковистостью. Длина технического волокна доходит до 3 ж, поперечник сечения элементарного волокна 10-26 ц, в среднем 18 Употребляется в ограниченных количествах для производства тонких тканей, сетей. См. Волокна. АНАНАСНАЯ ЭССЕНЦИЯ, смесь этило-масляного (30 ч.) и изоамило-изовалериа-нового (130 ч.) эфиров в спиртовом (840 ч.) растворе или смесь этиломасляного (50 ч.), изоамиломасляного (100 ч.), изоамилоук-сусного (10 ч.) эфиров, лимонного (1 ч.) и померанцевого (2 ч.) масел с глицерином (30 ч.) и спиртом (1 ООО ч.). Применяется для приготовления напитков и кондитерских изделий. АНАСТАТИЧЕСКОЕ ПЕЧАТАНИЕ, в типографском деле - печатание с форм, полученных путем хим. перевода на литографский камень или цинк ранее отпечатанных листов, во избежание расходов и потери времени, связанных с новым набором. А. п. применяется в случаях переиздания словарей, книг по математике, нот и других книг, набор к-рых сложен и дорог. Есть ряд способов А. п.; наиболее распространено печатание при помощи смачивания листов ранее отпечатанного издания слабым (5-10%) раствором азотной к-ты, после чего листы сильно притискиваются прессом к гладко отполированной поверхности литографского камня или цинковой пластинки. Азотная
|