
 |
|
|
Главная --> Промиздат --> Абразионные материалы Валик с основой IIIIIIIIIIIIIIII Ремизка 1 Гg 2 С= 3 (- 4 г Ткань Навой с готовой тканью  Бердо I I - щ! шш мм м1  п а Фиг. 1. Заправка ткани на основании результатов анализа. 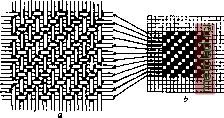 Фиг. 2. Определение саржевого переплетения: а-строение ткани, b-графическое ее изображение. 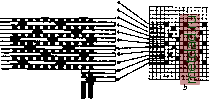 Фиг. 3. Определение атласного переплетения (уточного): а - строение ткани, b - графическое изображение перенлете1Н1я. 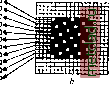 Фиг. 4. Определение атласного переплетения (основного): а -строение ткани, Ь- графическое изображение переплетения. т. э. оЛ.гвГУ.м.го.Цуи.ЕмПоим зевообразовательный механизм, а по системе зевообразовательного прибора приготовляется рисунок картона. 10. Определение веса ткани. Вес ткани зависит от рода материала (пряжи), ее №, плотности и структуры ткани. Для определения веса квадратного ярда или метра ткани служат: 1) квадрант Ланкастера (фиг. 6), который по образцу ткани в Vioo квад. ярда определяет вес 100 кв. ярдов ткани в lbs. (англ. фунт), 2) универсальный баланс Штауба и другие приборы. Определение веса единицы площади ткани заключается в следующем: по щаблону, прилагаемому к приборам, вырезают прямоугольник ткани, который и показания полу- 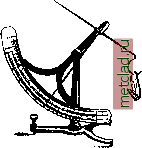 Фиг. 6. Квадрант Ланкастера. взвешивают на приборе; чаются по шкале. 11. Учет материалов в ткан и. Под учетом материалов в ткани подразумевается определение количества основной и уточной пряжи. Вес пряжи в куске определяется по следующим формулам: L.n , вес основы 6г = --7 к в кг, вес утка . 1 ООО l.aAOO.L 1000 в кг, где L-длина куска, п-число ниток в основе, к - коэффициент уработки основы, I - ширина основы в берде вм, а - число уточных прокидок на 1 см, - метрический № пряжи. Эти ф-лы справедливы для метрической нумерации пряжи. Лит.: Тихомиров м. С, Строение и анализ хлопчатобумажных тканей в связи со способами их изготовления, Ив.-Вознесенск, 1926; Архангельский А. г.. Волокна, пряжа, ткани, М., 1914; Л а п и с о в А. Г., Руководство по анализу и заправке тканей, Варшава, 1903; LecointreAch., Traite de 1 analyse des etoffes, Lille, 1905; Barker A. and M i d g 1 e у E., Analysis of Woven Fabrics, 2 ed., L., 1922; Taylor J. Т., Cotton Weaving a. Designing, 5 ed., L., 1905; Beaumont Rob., Standard Cloths, Structure and Manufacture, L., 1916; Bittner Em., Katechismus d. Bindungslehre, Verl. d. Вгиппег Monatsschrift f. Textilindustrie , Brunn, 1909-1914. C. Молчанов. АНАЛИЗ ХИМИЧЕСКИЙ, определение состава смеси веществ на основании хим. взаимодействий или физ .-хим. свойств. Разделяется на: 1) анализ качественный, ограничивающийся установлением наличия данного атома, иона, группы атомов или вещества, и 2) анализ количественный, устанавливающий относительное содержание данного атома, иона и т. п. в смеси веществ. Качественный анализ неорганич. веществ разделяется на анализ к а-тионов и анионов. Анализ катионов проводится систематически, благодаря возможности разделения катионов и атомов по группам: V- As, Sb, Sn-осаждаемые из кислых раство- ров сероводородом, но растворимые в многосернистом аммонии; IV-Hg, РЬ, Bi, Си, Cd-нерастворимые ни в кислых ни в щелочных растворах сероводорода и его солей; III -Мп, Fe, Ni, Со, Zn, AI, Cr - растворимые в кислых растворах сероводорода, но не растворимые в растворе сернистого аммония; II - Ва, Sr, Са - растворимые в присутствии (NH4)SH и осаждаемые аммиаком в присутствии углекислого аммония; I-Mg, К, Na-растворимые в присутствии аммиака и углекислого аммония. Особо стоят: а) группа серебра, свинца и закиси ртути, осаждаемая соляной к-той в виде AgCl, HgCl и PbClg (последний - неполностью), и б) аммиак, к-рый благодаря летучести открывается легко. Разделение металлов в каждой группе требует специальных приемов. В V группе пользуются: а) различием растворимости AsgSj, с одной стороны, и SbgSj, SnSg, с другой, в крепкой соляной к-те или в крепком растворе углекислого аммония и б) различием растворимости Sb и Sn в соляной к-те. В IV группе пользуются нерастворимостью HgS в азотной (20%-ной) к-те, PbSO* в крепкой серной к-те, нерастворимостью В1(0Н) 3 в аммиаке и интенсивно синим окрашиванием Си-аммиачных комплексов. В III группе возможно использовать нерастворимость CoS и NiS в нормальной НСР, остальные катионы этой группы, т. е. Fe, Сг, А1, Мп, Zn, молшо разделить друг от друга, пользуясь нерастворимостью Fe, А1, Сг, в виде основных уксуснокислых солей; или же соединения Fe, Со, Ni можно осадить путем взбалтывания их со свежеприготовленным ВаСОд. И в том и другом случае соединения Zn и Мп остаются в растворе. Кроме того пользуются различием растворимости гидратов окислов Ре(ОН)з, А1(0Н)з, Сг(ОН)з при действии на них щелочей в присутствии перекиси водорода; при этом переходят в раствор А1(0Н)з и Сг(ОН)з, из которых А1(0Н)з далее осаждается кипячением с NH4CI. Для II и I групп пользуются тем, что Mg, К, Na (I группа) растворяются в присутствииNH3hNH4HC03, а Ва, Sr, Са (II группа) от действия этих реактивов осаждаются в виде углекислых солей. Последние отделяют друг от друга благодаря различию растворимости их хромовокислых, сернокислых и щавелевокислых солей. В I группе Mg отделяют от Na и К, пользуясь различием растворимости гидратов окисей и нерастворимостью аммоние-вомагниевой двойной соли фосфорной к-ты. Ход анализа приходится избирать в зависимости от той или иной комбинации солей, присутствующих в анализируемой смеси. Весьма важными оказываются специальные реакции для обнаружения некоторых ионов; напр.: 1) для обнаружения в виде осадка иона К* используется ничтожная растворимость комплексной соли К3 [Co(N02)el (соль Фишера); 2) для определения ионов натрия пользуются очень малой растворимостью соли NagHaSbgO,; 3) ионы Cd распознаются по характерному желтому цвету осадка CdS; 4) для меди характерна интенсивная, густая окраска комплексного иона окисной аммиачной меди; 5) для хрома характерным является красивый синий цвет раствора надхромовой к-ты в серном эфире; 6) железо характеризуется очень интенсивно окрашенными комплексными солями: а) берлинской лазурью Fe4[Fe(CN)g]3, б) турнбулловой синью Рез[Ре(СМ)в]г и кровавокрасным цветом растворов роданового железа Fe(CNS)3 (или, вероятно, Нз[Ке(СМЗ)в]; 7) для Ni характерна нерастворимость комплексной соли дициандиамидина и никеля и нерастворимая и интенсивно окрашенная комплексная соль диметилглиоксима и никеля, который с C2H5N4O2 дает осадок или красное окрашивание в аммиачном растворе (то же и на закись железа); наоборот, соответствующая соль кобальта легко растворима; 8) для констатирования Со пользуются тем, что кобальтовая соль /3-нафтохиноксима трудно растворима, а никелевая хорошо растворима; 9) для разделения железа и меди от Zn, Ni, Мп, Со можно использовать то обстоятельство, что соли нитрофенилгидро-ксиламина (купферрона) - железная (красная) и медная (серая) почти полностью выпадают из уксуснокислого раствора, тогда как соли Zn, Со, Ni, Мп при этих условиях легко растворимы. Можно ожидать, что дальнейшее развитие химии комплексных соединений позволит нам использовать целый ряд комплексных солей для определения того или иного иона без предварительного отделения его от остальных. Вспомогательными действиями в ходе анализа являются: 1) нагревание в пробирке (заметны возгоны солей NH4 и Hg, красно-бурые пары из солей азотной к-ты); 2) нагревание при помощи паяльной трубки на угле с содой (корольки металла или налеты); 3) исследование окраски пламени, особенно характерной для солей Li, Sr, Си и др.; 4) окраска сплавленных со следами испытуемого вещества фосфорных стекол и стекол буры (т. н. перлов ), из которых особенно характерны зеленый цвет для хромовых соединений и синий цвет для кобальтовых соединений. Нагревание с крепкой или слабой серной кислотой позволяет подметить различие в анионах. Разделение последних на группы основано на взаимодействии с азотнокислым серебром и азотнокислым барием, но оно не м. б. проведено столь систематично, как для катионов. Характерны окраски бру-цина и особенно нитрона (дифенилэнданило-дигидротриазола), получающиеся в присутствии ничтожных количеств азотной к-ты, к-рую трудно определить методом осаждения в виду растворимости всех ее солей. Ход самого анализа зависит от того, в каком виде дано вещество. Прежде всего, если вещество дано в твердом состоянии, стараются его перевести в раствор действием солягтой или азотной к-т, смеси обеих к-т (царская водка), или сплавлением со смесью сернокислых калия и натрия, или действием фтористоводородной к-ты (в случае силикатов). Прежде всего определяют наличие аммиака (аммония) нагреванием вещества с едкой щелочью и действием выделяющихся газов на влажную лакмусовую бумажку или бумажку, смоченную со.тью закиси ртути. Еще до переведения вещества в раствор делают предварительные испытания при по- мощи паяльной трубки, нагревают небольшую пробу вещества в запаянной трубке и т. п. Систематический ход анализа ведут, строго соблюдая условия: 1) полноты осаждения, для чего иногда необходимо прибавлять раствор электролитов, чтобы нек-рые из нерастворимых составных частей вещества не прошли сквозь фильтр в состояшти т. н. коллоидного раствора (см. Коллоиды)-,2) полноты промывания, чтобы быть уверенным в том, что в осадке не остались примешанными или адсорбированными вещества, к-рым надлежит быть в фильтрате. В виду этого необходимо: а) анализ производить с возможно меньшим количеством веществ; б) промывание на фильтре или путем декантации вести возможно многими порциями растворителя, но каждый раз удаляя его, так чтобы в осадке оставалось возможгю меньше растворителя; в) проверять особо чувствительными реактивами отсутствие в фильтрате растворенных веществ, что укажет на полноту промывания; г) строго соблюдать выработанные практикой условия работы, т. к. несоблюдение их может совершенно исказить результаты; это наблюдается, напр., если в отсутствии электролитов при промывании осадка III группы часть железа перейдет во II группу. Систематический ход анализа катионов является важным не только сам по себе, но и как школа химической мысли, в к-рой начинающий химик учится пользоваться для отделения друг от друга индивидуальными, и притом часто незначительными, отличительными признаками отдельных атомов или ионов и вместе с тем знакомится с многосторонней характеристикой какдо-го из атомов и ионов. Количественный анализ в нек-рых отношениях ведется по тем же принципам, что и [качественный, однако не все приемы последнего одинаково удобны для количественных определений; напр., иногда мы можем качественно установить присутствие того или иного элемента, пренебрегая при этом малой, но все-таки заметной, растворимостью соли данного элемента, количественное же определение его в таких случаях повлечет за собой значительную ошибку. Поэтому при количествегшых определениях приходится комбинировать ход анализа несколько иначе, чем при качественных. Кроме того практически при количественных определениях редко приходится встречаться с необходи.мостью .методических разде-тений сложных смесей. Обычно задача количественного опреде.тения значительно проще, в виду того, что предварительно делается качественный анализ. Основой количественного анализа является весовой анализ, пользующийся методом точного взвешивания исходного вещества и получаемых соединений того элемента, содержание к-рого мы хотим определить. При этом необходимо, чтобы полученное в виде осадка соединение выделялось в хорошо образованных и не слишком мелких кристаллах и чтобы кристаллы были устойчивыми или же чтобы они могли быть доведены путем продолжительного прокаливания до постоянного веса. Напр. серную
|