
 |
|
|
Главная --> Промиздат --> Абразионные материалы действием w-толуолсульфохлорида и отделяют пары диэтиланилина от нелетучего эфира, к-рый разложением концентр, серной к-той переводят снова в моноэтиланилип. Лит.: Ворожцов Н. Н., Ступени в синтезе красителей. Л., 1926. АЛКИЛИРОВАНИЕ, процесс введения углеводородных остатков - алкилов или арилов--в различные хим. соединения. А. осуществляется двояким способом: 1) путем замены атомов водорода алкилами или 2) присоединением галоидных алкилов или алкильных эфиров минеральных кислот к органическому, реже к неорганич. соединению. Так, напр., образование первичного амина из аммиака и галоидного алкила относится к первому типу, а образование четвертичного аммониевого основания-ко второму. В результате А., в зависимости от природы алкилируемого вещества, получаются эфиры простые и слолсные, замещенные амины, аммониевые основания и ряд других соединений, имеющих разнообразное применение в технике. Чаще всего А. пользуются для замены атома водорода, находящегося при кислороде (водород гидроксила) или при азоте органического вещества, иногда при углероде. Последний случай имеет место только в таких соединениях, где водород обладает большой под-вилшостыо, напр., в малоиовом и ацето-уксусном эфирах и т. п. С техиич. точки зрения наибольшее значение имеют мети льпая, этильная и бензильная группы; введение других алкилов происходит довольно редко. Для А. пользуются различными соединениями, из к-рых важнейшими являются: ал к оголи (метиловый и этиловый), галоидные алкилы (хлористые метил и этил, реже их бромистые и йодистые производные), эфиры серной к-т ы (диметил- и диэтилсульфат) и эфиры арилсульфоновых к-т (метиловый и этиловый эфиры п-толуолсуль-фокислоты). Метилирование помощью ч е-твертичных аммониевых оснований, или диазометана, имеет место только в специальных случаях. А. с о е д и н е н и й с г и д р о к с и л ь-ной функцией (замена водорода при кислороде) часто посит название э т е р и-ф и к а ц и и и служит способом получения простых эфиров. Способ состоит в том, что алкоголь (для получения смешанных эфиров - смесь из двух алкоголей) нагревается в присутствии серной к-ты, которая играет роль катализатора. Простейшим примером этерификации может слулшть получение серного эфира из этилового спирта. Другой способ А. спиртов состоит в том, что соответствующий алкоголят натрия подвергается обменному разложению с галоидным алкилом: RONa-fClCHg-ROCHs+NaC]. Для А. фенолов пользуются галоидными алкилами или, лучше, диметил- или диэтилсульфатом, которые реагируют при взбалтывании с водными или водноспирто-вым раствором фенола, выход эфира при этом почти количественный (см. Анизол). Вследствие большой ядовитости диметил-сульфата, в последнее время в технике стали применять эфиры арилсульфоновых к-т и, в первую очередь, метиловый эфир ti-толу-олсульфокислоты. Некоторые производные фенолов, напр. нитрофенолы, чрезвычайно трудно обменивают свой водород на алкилы. В этих случаях А. лучше вести помощью галоидных алкилов, в присутствии едких щелочей, нагреванием в автоклавах под давлением. Такой способ применяется, напр., для получения о- и w-нитроанизола. Нафтолы алкилируются легче, чем фенолы; для получения, напр., метилового эфира -нафтола (см. Неролин) достаточно 4-часового нагревания при 125° раствора -нафтола в метиловом спирте в присутствии небольшого количества серной к-ты. Для А. веществ со слониной химической функцией, например алкалоидов, иногда псльзу-ются четвертичными аммониевыми основаниями, из которых особого внимания заслу-лшвает гидрат окиси фенилтриметиламмония (ОН) N(CeH5) (СНз)з - вещество, применяемое в технике для получения кодеина из формия. Реакция протекает по схеме: R- он + OH-N C.Hs (СН,)з -> R0 N С<Д, (Clhh -> ROCH3 + N С.Н5 (СНз)2. А. азотистых органич. соединений, как выше было указано, происходит двояким образом: заменой атома водорода амиио-или имино-группы алкилами и путем присоединения галоидных а.11килов к третичному атому азота; последний процесс приводит к образованию солей четвертичных аммониевых оснований. К третичным аминам лсирного ряда легче всего присоединяются йодистый метил и диметил сульфат, тогда как для присоединения хлористых или бромистых алкилов требуется нагревание, . Образование четвертичных аммониевых оснований в ароматическом ряду происходит еще легче, чем в жирном. Так, напр., йодистые или бромистые алкилы присоединяются со значительным разогреванием, и для того, чтобы реакция шла тише, необходимо прибегать к парулсному охлаждению и вести реакцию в среде индифферентного растворителя. Диметилсульфат и эфиры п-толуолсульфокислоты реагируют еще более энергично. Этот способ имеет применение в производстве органич. красителей. Для метилирования т, н. кислой имид-ной группы, например в анилидах, особенно пригодны эфиры арилсульфоновых кислот и диалкнлсульфаты. Замена амин-ного водорода в ароматич. аминах легко осуществляется нагреванием соответствующего амина с этиловым или метиловым спиртом в присутствии серной кислоты. Этим путем в технике получаются диметиланилин и другие алкиланилины. Для бензи-тирова- НИЯ аминов пользуются почти ИСК.Т10ЧИ- тельно хлористым бензилом (см. Бензил хлористый). А. представляет собою операцию, к-рой часто пользуются в технике для получения синтетических красителей, лекарственных, душистых веществ и других органических препаратов. с. Медведев. АЛ к ил Ы, общее название одновалентных радикалов углеводородов ншрного ряда; отдельные названия А. составляются из соответствующего названия углеводорода с изменением окончания а и на ил: А. метана- метил СНз, А. этана - этил СИ-ь, и т. д. АЛКОГЕЛЬ, студень, в котором вода заменена спиртом; для желатиновых и агаровых водных студней превращение в А. легко достигается погружением их в спирт постепенно увеличивающейся крепости, пока не произойдет замена воды спиртом. Твердость такого А. выше, чем водного геля (студня); при высушивании он становится непрозрачным и напоминает собою мел, в виду того что в поры геля на место испаряющегося спирта входит воздух. См. Коллоиды. АЛКОГОЛЕМЕТРИЯ, определение содерлсания спирта в спиртных жидкостях (водке, пиве, вине и пр.). Если жидкость не содержит ничего кроме алкоголя и воды, то определение производится по уд. весу. D чистого спирта 0,79425. Уд. вес вод- ного раствора спирта заключается между 0,79425 и 1 и тем больше, чем меньше в нем спирта. Содержание спирта в лсидкости выражается в весовых или в объемных %, т. е. числом 8 алкоголя в 100 г раствора или числом см алкоголя в 100 см раствора. Найдя уд. в., содержание спирта (в объемных и.ти в весовых %) определяют по таблицам, к-рых имеется несколько, состав-тенных разными авторами. Как видно из приложенной сокращенной таблицы, весовые и объемные % не совпадают. Это зависит не только от того, что спирт и вода имеют разный уд. в., но еще и от того, что при смешении спирта с водой происходит сжатие. Если, например, смешать 100 л воды и 100 л спирта, то получим не 200 л смеси, а только 192,8 л. Т. к. в ней содержится 100 л алкоголя, то его будет 51,8% (в объемных %). Т. к. 100 л алкоголя при 15° весят 79,367 кг, а 100 л воды 99,914 кг, то 192,8 л смеси весят 179,281 кг; следовательно, в ней содержится чистого алкоголя 44,27 весовых %. Определение уд. в. производится обычно при помощи пикнометра или весов Мора-Вестфаля, или же при помощи ареометра, при чем в данном случае применяют специальные ареометры - стеклянные спиртомеры, у которых деления обозначают не уд. в., а прямо % алкоголя. У нас применяется спиртомер Траллеса (фиг. 1), у к-рого деления обозначают объемные %. Определение производится при 15°, 5. Спиртомер Траллеса состоит из полого стеклянного цилиьщра, оканчивающегося вверху трубкой с бумажной шкалой, а внизу - шариком с грузом (ртутью, дробью), удерживающим спиртомер в вертикальном положении. Обычно в цилиндриче-Фиг 1 ой части устраивается термометр, спирто- шарик к-рого служит одновременно мер и грузом для спиртомера. Т. к. по-саказаиия спиртомера правильны только при 15°,5, то для других t° необходима поправка по таблицам, прилагаемым к спиртомеру. К официальному употреблению у нас принят металлический спиртомер (фиг. 2), показывающий также объемные % 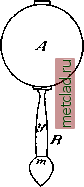 Фиг. 2. Металлический спиртомер. алкоголя. Он состоит из медного, вызолоченного шарика А со стержнями Б и В. Нижний стержень несет груз ш, а верхний снабжен делениями от О до 10, с подразделениями каждого на 5 частей. К спиртомеру прилагается 10 гирек, обозначенных числами О, 10, 20, 30, 40, 50, 60, 70, 80 и 90, к-рые могут навешиваться па утончзнную часть у нижнего стерлшя. Спиртомер погружают в спиртовую жидкость, налитую в стеклянный цилиндр, и отмечают деление, до к-рого он погружается. Если спиртомер не погружается до нижнего деления, то навешивают ту или другую гирьку так, чтобы уровень жидкости пришелся между верхним и нижним делениями шкалы. К показаниям спиртомера прибавляют число, показанное на гирьке, а если он достаточно погружается без гирьки, то прибавляют 100. Так, если спиртомер погрузился до уровня мп без гирьки,то его показание будет 109,6; если же он погрузился до этого деления с гирькой, обозначенной 60, то его показание будет 69,6. Если уже без гирьки спиртомер погружается выше верхней черты, то жидкость надо охладить, поставив цилиндр в воду со льдом, чтобы она сделалась плотнее и спиртомер поднялся. Найдя показание спиртомера и измерив t° жидкости, по прилагаемым табл. отыскивают истинное Определение содержания алкоголя.
ставных частей. Берут 200 см жидкости, отгоняют от нее в перегонном аппарате объема, в которые переходит весь алкоголь, дополняют отгон водой до первоначального объема и получают т. о. тот же объем нсид-кости, который был взят, но в котором содержится только алкоголь и вода. Определив теперь уд. в, жидкости, находят по таблицам содержание в ней алкоголя, или же прямо измеряют крепость жидкости помощью спиртомера. Для быстрого, хотя и менее точного, определения алкоголя, 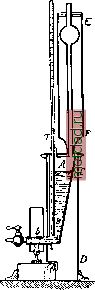 Фиг. 3. Эбуллио.метр Салеропа. содержание алкоголя в объемных %. Показания спиртомера, или объемные %, у нас называются градусами . Так, напр., хлебное вино с содержанием 40 объемных % алкоголя называется вином в 40° крепости, или 40-градус11ым вином. Вместе с тем градусом называют также Vioo часть ведра при 15°,5, которая служит единицей для учета количества спирта. Если, напр., мы имеем партию 40-градусиого вина в 158,5 вд., то количество безводного алкоголя в ней будет 158,5x40 = 6 340° (63,4 вд.). В настоящее время для учета безводного алкоголя в спиртосодержащих жидкостях у нас вводится метрическая система, применяемая в других европ. государствах, название градус отменяется, крепость спиртосодержащих жидкостей выражается в объемных % нри 15°, единицей для количественного учета служит л безводного алкоголя нри 15°, оптовой единицей принимается 1 гл. Если в лсидкости содержатся, кроме спирта и воды, и другие составные части (нелетучие), как, напр., в пиве, вине, бражке и т. п., то в этом случае необходимо предварительно отделить отгонкой спирт от других со- гл. обр. в винах, пользуются эбуллиометром Салеропа. Устройство его основано на том, что смеси спирта с водой кипят при определепной t°, точно зависящей от содержания в них спирта. Прибор состоит из резервуара А (фиг. 3), нил-сний конец которого соединяется с гори-зоетальной трубкой Ъ, служащей для нагревания. Резервуар для предохранения от охлаждения окружен кожухом CD и снабжен обратным холодильником EF и термометром Т, со шкалой, разделенной на десятые доли градуса. В резервуар А наливают нек-рое количество дистиллированной воды (15 см), нагревают ее до кипения и замечают Г на термометре. Положим, она равна 100°,2. Тогда на прилагаемой к прибору линейке (фиг. 4) устанавливают подвижную (среднюю) шкалу так, чтобы число 100,2 совпадало с нулем неподвижных шкал А и В, и закрепляют ее винтом Е. После этого, вылив из резервуара воду и сполоснув. Фиг. 4. Линейка к прибору Сале-рона.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||