
 |
|
|
Главная --> Промиздат --> Абразионные материалы типа А. и содернащаяся между 1,2 и 1,8. Ф-ла Пейкерта имеет силу только для разрядок постоянным током. Эта ф-ла применима к свинцовым А. любого типа с точностью 1 - 2%. Для быстрого вычисления отношения емкостей Са: Сх по заданному соотно- 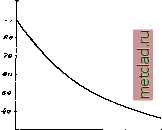 о /о яо до Сила разрядного тока so А Фиг. 11. Емкость аккумулятора в зависимости от силы разрядного тока (примерная кривая). шению соответствен, времен разрядок и Tl и характеристичному числу п-или, наоборот, для нахождения числа п по отношению емкостей С : С, и отношению соответствен, времен разрядок : служит табл .9. Табл. 9.-Д анные Ф. Лоппе для применения формулы Пейкерта.
Зависимость емкости от концентрации электролита. Емкость А. возрастает с концентрацией кислоты до некоторого максимума и затем убывает. По Долезалеку, максимум емкости совпадает с концентрацией наибольшей проводимости кислоты (30%, уд. в. 1,224). Однако, по Жюмо, оптимальная концентрация зависит от режима разрядки и, кроме того, различна для анодов и катодов (табл. 10). Табл. 10.-3 а в и с им о с т ь концентрацип от режима разрядки.
Эти данные имеют значение лишь примерное и относятся к определенному типу пластин. Зависимость емкости А. от такова, что можно считать нарастание емкости, сравнительно с таковою же при ° 15°, примерно в 1% на 1°. Однако повышение емкости посредством повышения t° не рекомендуется, т. к. это разрушает электроды (катоды) и усиливает местные действия, а получаюшиеся потери при очень медленных разрядках приводят к нулю выгоду увеличения емкости нагреванием. Возрастание емкости с t° объясняют увеличением при нагреве проводимости и диффузии электролита. Увеличение емкости от повышения f тэм более значительно, чем быстрее разрядка. Оно зависит также от типа пластин, от предшествующих разрядок, от концентрации кислоты и различно для катодов и для анодов. 10. Отдача А. Отдача электричества ?7д свинцового А, при наилучших условиях достигает 0,90 и даже 0,95 (т. е. 90-95%); она мало зависит от увеличения силы тока и от концентрации электролита. Потеря в 10-5% обусловлена гл. обр. местными действиями, особенно при длительном отдыхе после зарядки. При расчетах j? принимается равным 0,9. У щелочного А. отдача равна 0,72-0,80. Саморазрядка. А. обычного типа при хорошем содержании теряют не менее 1% своего заряда в сутки; А. же загрязненные не держат своего заряда, и потеря их может доходить до 50% и более. Даже наилучшие современные А. за месяцы отдыха дают 40-60% потерь. Страдают от потери преимущественно катоды,-как по- , (,oi казывают графи- 1::оэ ки (фиг. 12), через 120 суток в опытах Жюмо ка- ч,о.5 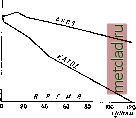 Фиг. 12. тод потерял весь заряд, а анод-1] только 25%. Но, ai при возможном устранении местных действий, в А. Фери достигнута весьма малая потеря заряда, а именно: 5-7% в первый месяц после зарядки и средним числом 3% в последующие. Источником саморазрядки А., обусловливающим местные действия, ранее считали птатину; теперь, когда серная кислота готовится без платины,-железо, к-рое Служит передатчиком кислорода от анода к катоду. Однако главная причина потери заряда - кислород воздуха, вызывающий самопроизвольную сульфацию катода, согласно двум реакциям: H2S04-bPb=PbSO,-fHj и H2-fO = HjO. Этот процесс усиливается от прохождения пластин через слои электролита с разной концентрацией растворенного воздушного кислорода. Поэтому горизонтальное помещение катода на дне бака дало в А. Фери (фиг. 13) превосходную меру борьбы с саморазрядкой, и на разработку этого принципа д. б. направлено внимание конструкторов. Напротив, рекомендованное недавно прибавление к электролиту щелочного бисульфата не оказывается полезной мерой; кроме того, вследствие некоторой растворимости сернокислого свинца в сернокислых щелочных металлах, оно может ускорить разрушение пластин. Отдача энергии при наилучших условиях колеблется между 0,75 и 0,85 (75-85%); на ибольшее значение ее при 30%-ной кислоте (уд. вес ок. 1,22). При расчетах rjjg принимается равным 0,75-0,82; ? <?д(ск-рой связано соотношением = Vq), потому что коуфф. понижения > 1. Так как с повышением t° Jjq убывает, а А возрастает, то мало зависит от t°. При той же отдаче электричества отдача энергии возрастает с концентрацией электролита и убывает при возрастании тока. При разрядке А. теряет энергию в форме теплоты; это, однако, не длоулев-ская теплота, а теплота происходящего от нескольких причин смешения кислоты разных концентраций. Потеря энергии, вызванная токами соотношением:  Фиг. 13. Сухой аккумулятор Фери. концентрации, выражается (22) в вольт-кулонах, где а - константа, Ъ - конструктивная постоянная пластин, - средняя проводимость кислоты. В первом приближении молено считать Ь/Д , независящим от /, так что W= aI4. (23) В силу пропорциональности W квадрату силы тока потерю энергии в первом приближении можно рассматривать условно как джоулевское тепло, но при возросшем внутреннем сопротивлении, У щелочного А. отдача энергии 0,52-0,55, II, Технические факторы емкости. Использование материала электродов в свинцовых А, опреде- ляется следующими данными: не все активное вещество обслуживает зарядку А,; отношение между массой вещества, действительно дававшего емкость, и полной массой активного вещества называется коэфф. использования. Очевидно, при тех же самых опытньгх данньгх, коэфф. использования окажется различным в зависимости от принятой эл,-хим, схемы А, Имеющиеся данные приведены и в табл. 11 и 12. Табл. 11. - Данные для вычисления практич. достижимого коэфф. использования свинцового А.
Значение диффузии. Использование активного вещества ограничено недостаточным притоком кислоты внутрь пластин. Заставляя проникать кислоту в катод под давлением, Либенов получил емкость А. в три раза большую, чем без давления. Отсюда вытекает необходимость по возможности увеличивать пористость активной массы, в частности-тонкостью ее кристаллов. Проникновению кислоты способствует также малая толщина пластинок; по приближенной ф-ле Либенова где С-емкость А. с электродами из одного и того же количества активного вещества, h - толщина пластин, а и /S - постоянные. Однако недостаточная механическая прочность слишком тонких пластин и быстрая их изнашиваемость эл.-хим, процессом ставит предел увеличению емкости путем дальнейшего утончения. Долговечность пластин. Положительные пластины большой поверхности сперва работают своею пастой. Емкость их возрастает до нек-рой наибольшей Табл. 12. - Данные для вычисления максимального использования свинцового А. коэффициента
величины и затем держится неизменной, пока отпадение пасты возмещается превращением в перекись ребер. Затем, после полного преобразования этого материала, емкость постепенно убывает до полного изнашивания электродов. Пастированные пластины ведут себя различно, в зависимости от нх пористости и молекулярного состояния. Отрицательные пластины по емкости превосходят полонительные, но вскоре, из-за слсатия свинца, пористость и проводимость пластин уменьшается, и емкость убывает, сперва довольно быстро, затем медленно, при чем активное вещество дает трещины. Попытка устранить это явление прибавкой к свинцу инертных материалов не имела полного успеха. В общем, все приемы увеличения уд. емкости сокращают срок слулбы электрода. Аноды Аккумуляторного треста выдерживают 108 - 150 зарядов, катоды-несколько больше. При хорошем уходе аноды станционных батарей служат 5-6 лет, а катоды- до 10 лет. Германские аккум. батареи высокого напрялсения для радио в лучшем случае могут работать 2 - 3 года. Табл. 13. - X а р а к т е р II с т II к а Сурьмянистый свинец более прочен механически и менее окисляем, чем чистый. Обыкновенно он содержит 6-12% сурьмы. Сп.тавы РЬ менее чем с 13% Sb имеют t°nA. ниже, чем каждый из компонентов; сплав с 13% Sb остается жидким до 228°. Понижение °пл. пропорционально содержанию сурьмы и может служить для вычисления этого содержания. Точно так же уменьшение уд. в. сплава пропорционально содержанию сурьмы и, начиная от 11,35 для чистого свинца, составляет 0,074- 0,072 на 1% Sb. Изготовление сплавов производится двумя способами: если требуется большое содержание Sb, то сурьму расплавляют в графитовом тигле, дают охладиться до t°ome., прибавляют часть расплавленного свинца и полученный сплав смешивают со свинцом, расплавленным в чугунном тигле; если же со;у.ержание Sb должно быть невелико, то в свинец, находящийся в чугун-пом тигле при 500°, прибавляют куски сурьмы и размешивают их до растворения. Свинцовые соединения. В аккумуляторном деле применяются соединения РЬ; сводка данных о них дана в табл. 13. свинцовых соединений д л я А. Соединения Ф-ла Молекул, вес Удельный вес гптгттри J пульверизованный...... Свинец губчатый........... Окись свинца, или глет........ Сурик .................. Двуокись свинца, называемая (неточно) перекисью............. Свинец сернокислый окисный..... Свинец углекислый........... Свинец хлористый ........... Свинец сернокислый недокисный . . . Перекись свинца, или надсвинцово-кислый ангидрид ........... РЬО РЬ.О. PbOs PbSOi PbCOa PbCU PbaSO. Pb,Os 223 685 239 303 267 278 510 абсол. 11,4 9-9,5 8,5-9,5 7-9 6,2 5-6 5,7 кажущ. 5-6 3-4 4-4,5 4-4,5 3 , 5-4 , 5
II. Производство аккумуляторов. . 12. Сырье для свинцовых А. С в и н е ц - главный материал производства свинцовых А. В дополнение к описанию его свойств (см. Свинец) отметим: линейный коэфф. усадки при затвердевании-ок. 0,01. Органические кислоты (уксусная, винная, щавелевая и др.) растворяют его. Из загрязнений рыночного свинца главные: цинк, сулема, мышьяк, медь, железо, серебро, олово. Переходя в раствор в А. и осаждаясь на катоде, эти соединения вызывают местные действия. Особенно опасны в качестве примесей металлы платиновой группы: 0,0001% их может вызвать саморазрядку А. в течение двух часов. Рафинированный свинец должен содержать 99,95-99,98% чистого свинца. Количественный анализ производится либо химически, либо электролитически. К лучшим маркам свинца относится английский свинец фирмы Куксон и Мак-Ланг. Сурьма применяется для составления сплавов со свинцом. Рыночный товар содержит 97,5-98,8% чистой сурьмы, а электролитическая-99,98%. Главные примеси: S, As, РЬ, Fe и Си. В виду сп.чавления сурьмы почти со всеми металлами, ее следует плавить исключ. в графитовых тиглях. Свинцовые соединения могут содержать различные вредные примеси для аккумуляторного дела: железо, марганец, медь, хлор, уксуснокислые соединения и азотистые. К сурику подмешиваются охра и толченый кирпич, а к другим соединениям-мел, сернистый барий и свинец. Связывающие вещества. К смеси свинцовых соединений прибавляются для образования пасты различные вещества; приводим список главнейших из них. Главные связывающие средства для настовых смесей. Кислоты и их соли. Серная кислота и сернокислые соли щелочных и щелочноземельных металлов (К, Na, NHj, Са, А1, Mg). Кислоты сернистая и гипосернистап. тионовая и тиосульфаты щелочных металлов. сульфоновая. фосфорная. щавелевая и щавелевокислый аммоний. уксусная и уксуснокислый свинец. феноловая и фенолят свинца. -> мочевая и сернокислая мочевина. пикриновая. Основания, окиси и минера.льные соединении. Едкое кали и едкий натр. Нашатырный спирт. , Окиси алюминия и магния. Квасцы, марганцовокислый калий. Насыщенная кислородом вода.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||